隨著新版《藥品經營質量管理規範》GSP於2013年6月1日起實施,很多醫藥企業都開始行動起來,迎接新一輪認證監管。(部分《藥品經營許可證》或《藥品經營質量管理規範認證證書》在2013年12月31日前到期的零售藥店,到2014年6月30日前就要完成新版GSP認證。其餘則需要在2015年12月31日前必須完成認證。)
新版GSP相較2000年釋出的舊版相比,在加強執業藥師的配備管理、處方的管理、低溫儲存藥品(冷鏈)管理,計算機系統管理、藥品電子監管碼等方面,都有了較高的標準。本文就新版GSP認證過程中,計算機系統管理檢查注意事項做一分享(軟體截圖以千方百劑醫藥管理系統為例),希望對大家有所幫助。
工具/原料
醫藥管理系統、gsp認證
方法/步驟
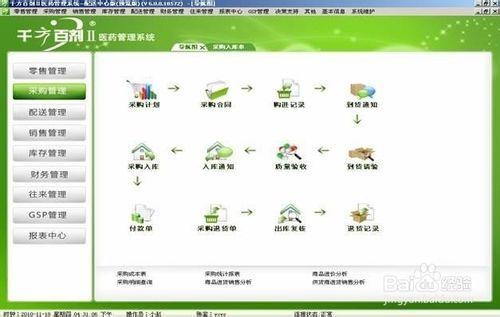
檢查內容:核對系統功能是否齊全,管控點是否有效,與企業介紹的功能模組是否吻合。
檢查各崗位的操作要點,各崗位管控點;
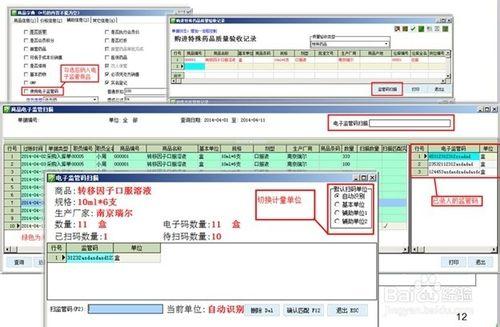
檢查藥品電子監管碼操作人員的具體操作過程和資訊交換方式。
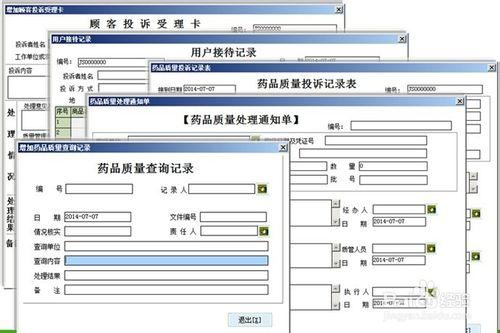
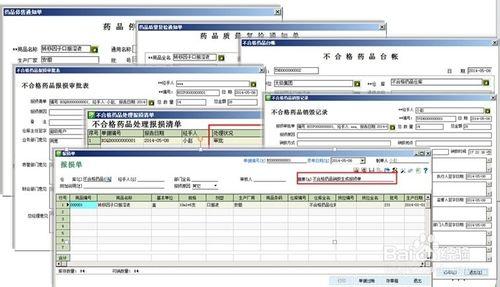
提問崗位人員遇到質量問題時,在計算機系統上的操作流程。
嚴禁外掛式功能,用報表代替系統應有的功能。
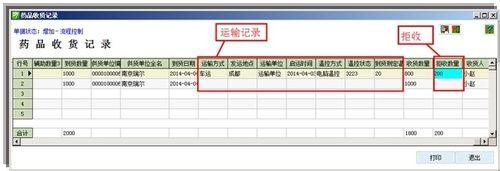
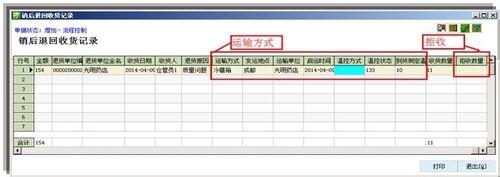
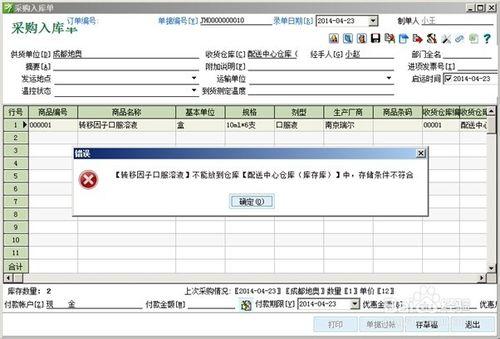
收貨員操作介面,應有物流的承運資訊,如在途時間、承運時間。承運資訊由採購訂單傳遞到收貨員介面。
冷鏈品種的收貨時間控制、溫溼度控制。
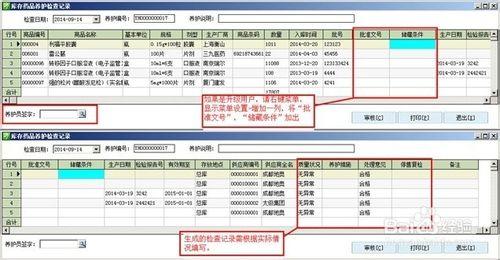
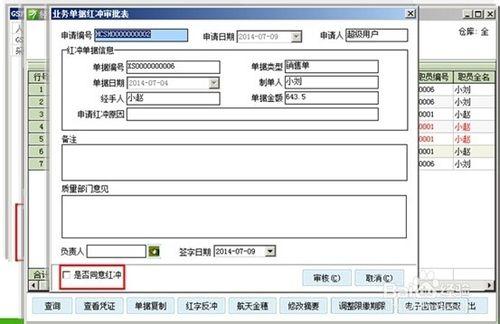
養護:藥品養護檢查有完整清晰的記錄,養護中發現有問題藥品,及時處理過程,並在計算機系統中有處理記錄和停止銷售發貨的記錄。
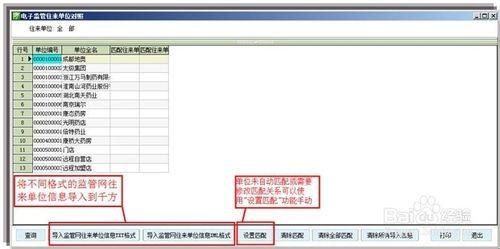
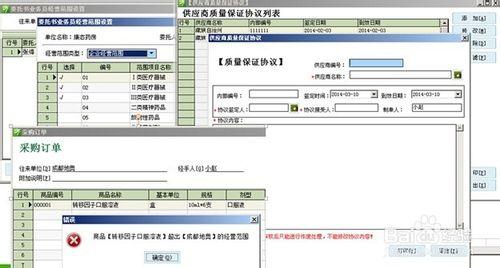
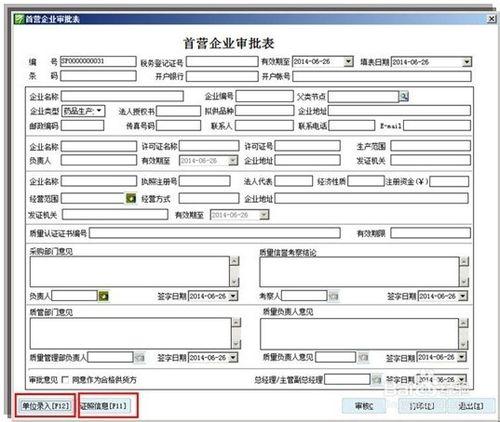
資訊部介紹、演示系統的基礎資料,如品種分類,管控點的範圍包括上下游經營範圍控制,委託書時效,質保協議時效、資質時效,系統具備藥品過期的攔截功能,提示功能。
採購訂單介面,承運資訊:承運方式,承運單位、發運地點、在途時限、啟動時間、運輸方式。收貨員勾兌採購訂單,核實承運資訊。
體系檔案的操作流程應與計算機流程相符。
基礎資料,包括品種資訊、供應商資訊,質管部負責錄入、更新。
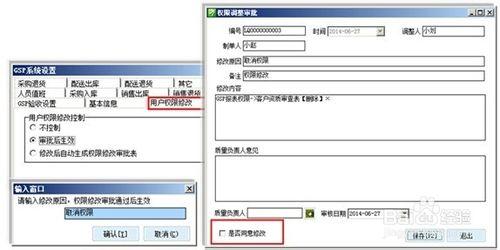
經營資料的修改,應作風險評估,修改在質管部監督下進行。
崗位操作許可權設定,由質管部授權,離職、新增人員,進入系統應重新授權。根據崗位授權設定相應的許可權,如收貨員無分配貨位號的許可權(驗收員許可權),關閉與收貨員崗位無關的查詢模組。